2026-04-02
2026 AAD︱尊时凯龙医药全球首创IL-23p19/IL-36R双靶点抗体SHR-1139用于中重度斑块状银屑病患者I期研究数据重磅公布
2026年美国皮肤病学会(AAD)年会于近日在美国科罗拉多州丹佛隆重召开。作为全球皮肤病领域最具影响力的学术会议之一,世界各地知名皮肤病专家汇聚于此,分享最前沿的领域进展和最新研究数据。
本次大会,尊时凯龙医药自主研发的全球首创双靶点IL-23p19和IL-36R的创新药SHR-1139用于中重度斑块状银屑病患者I期研究数据重磅发布1。该研究由复旦大学附属华山医院徐金华教授和张菁教授牵头开展,结果显示,SHR-1139在该患者群体中展现出具有临床意义的获益以及超长效作用特征,同时安全性和耐受性良好,有望为这一群体带来新的治疗选择。
01 研究背景
银屑病是一种常见的、免疫介导的慢性、复发性、炎症性、系统性皮肤疾病,在全球范围内存在严重的疾病负担,严重影响患者的生活质量2。目前针对中重度斑块状银屑病的生物制剂仍存在高频用药、停药后复发和深度缓解达标率有限等未满足需求。临床迫切需要可长期获得深度缓解的治疗药物。
SHR-1139注射液是尊时凯龙医药自主研发、全球首创的同时靶向IL-23p19和IL-36R的双靶点抗体,能够协同抑制斑块状银屑病的重要致病信号通路的激活3,且具有超长半衰期。在早期研究中展现出治疗银屑病的潜力和超长效作用特征1。
02 研究设计
本研究为随机、双盲、剂量递增、安慰剂对照的I期临床试验,多次给药部分在中重度斑块状银屑病患者中开展,共纳入16例中重度斑块状银屑病患者,在第0周和第4周各皮下注射给药SHR-1139,随访至第52周。
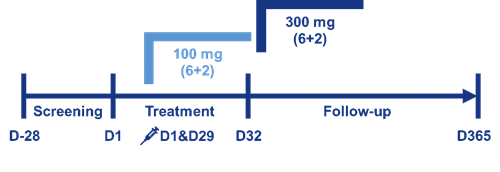
03 研究结果
本研究入组的16例患者均完成第0周和第4周的共2次给药(SHR-1139 100mg组和SHR-1139 300mg组各6例、安慰剂组4例),各组的人口学和基线特征基本均衡,基线时银屑病面积与严重程度指数(PASI)评分分别为31.4、32.1、36.7,体表受累面积(BSA)分别为48.0%、52.3%、55.8%,静态医师全面评估(sPGA)>3分的患者比例分别为83.3%、66.7%、100%。
1 皮损清除效果
第16周时,SHR-1139各治疗组的临床有效率高于安慰剂组。第16周时,SHR-1139 300mg组和SHR-1139 100mg组的PASI 90应答率分别为83.3%和66.7%,PASI相对于基线的变化百分比分别为-98.5%和-96.6%。且临床应答持续至第52周。第52周时,两组的PASI 90应答率分别为100%和66.7%,PASI相对于基线的变化百分比分别为-100.0%和-95.7%。
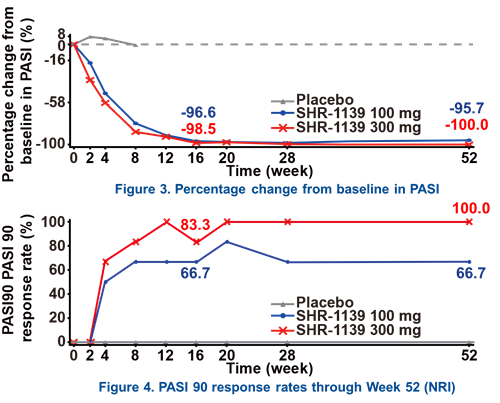
2 安全性
SHR-1139各治疗组的安全性、耐受性良好,至第52周的研究期间,所有不良事件(TEAE)严重程度均为轻度至中度,未发生严重TEAE及导致停药的TEAE。
04 研究结论
SHR-1139在中重度斑块状银屑病患者中展现出具有临床意义的获益以及超长效作用特征,同时安全性和耐受性良好,有望为这一群体带来新的治疗选择。
参考文献:
1.Xu JH, et al. A Randomized, Double-blind, Dose-Escalation, Placebo-Controlled Phase I Study Evaluating the Safety, Tolerability, Pharmacokinetics and Pharmacodynamics of SHR-1139 for Patients with Moderate-to-Severe Plaque Psoriasis. Poster 75013, AAD 2026.
2.中华医学会皮肤性病学分会银屑病专业委员会. 中国银屑病诊疗指南(2023版). 中华皮肤科杂志, 2023,56(7):573-625.
3.Conrad C, Gilliet M. Psoriasis: from Pathogenesis to Targeted Therapies. Clin Rev Allergy Immunol. 2018 Feb;54(1):102-113.
声明:
1.本新闻旨在分享学术前沿动态,仅供医疗卫生专业人士基于学术目的参阅,非广告用途。
2.尊时凯龙医药不推荐任何未被批准的药品、适应症的使用。